
- 高级人才招聘
- 中、初级专业技术人才招聘
- 管理、支撑岗位招聘
- 博士后招聘
植物依赖多层免疫系统应对病原体入侵。在抗病毒免疫中,核苷酸结合富亮氨酸重复受体(NLR)作为核心识别元件,负责感知病毒蛋白或病毒引起的宿主扰动。然而,免疫识别如何转化为直接限制病毒复制的执行机制,仍有待进一步阐明。
近日,中国科学院微生物研究所叶健团队在Journal of Integrative Plant Biology(JIPB)上发表题为“From recognition to proteolytic control: NLRs and metacaspases in plant antiviral immunity”的综述论文,提出了一种新型的植物抗病毒框架,即通过植物免疫的“识别-执行”双层框架:由NLR介导免疫识别,由半胱氨酸蛋白酶metacaspases(MCs)介导蛋白酶切执行过程。
在识别层,首个被克隆的抗病毒NLR基因N通过编码蛋白间接感知烟草花叶病毒(TMV)复制酶p50结构域触发免疫反应。随后研究表明,番茄Sw-5b识别番茄斑萎病毒(TSWV)运动蛋白NSm,辣椒Tsw识别病毒沉默抑制子NSs,马铃薯Rx1识别马铃薯X病毒(PVX)外壳蛋白CP。不同类型NLR的激活均伴随胞质Ca2+显著升高,为连接下游Ca2+依赖效应模块提供关键信号基础。
在执行层,MC4作为Ca2+依赖性蛋白酶,其活性由linker区自抑制,并在Ca2+诱导的构象变化与自剪切后逐步释放。在抗病毒免疫中,研究揭示了多条MCs依赖的调控路径:MC4切割免疫调节蛋白BAG3,诱发细胞死亡,从而抑制双生病毒侵染;MC4切割RNA结合蛋白La1蛋白,调控翻译过程,限制大麦条纹花叶病毒(BSMV)侵染;MC1切割自噬蛋白Beclin1,激活自噬通路以清除BSMV。这些发现表明,MCs并非引发非特异性蛋白降解,而是通过精准切割底物,将细胞组分转化为抗病毒分子。
尽管目前尚缺乏特定NLR通过Ca2+信号直接激活特定MC的明确证据,但基于现有研究,提出如下模型:NLR介导的识别层产生Ca2+信号,MC将其转化为持续的蛋白酶切过程,从而驱动抗病毒免疫执行过程。鉴于病原体常通过效应蛋白抑制宿主蛋白酶以逃避免疫,直接工程化免疫执行层可能成为抗病育种的重要策略。综上,NLR–MC的“识别-执行”框架为理解植物抗病毒免疫提供了一个新的视角。
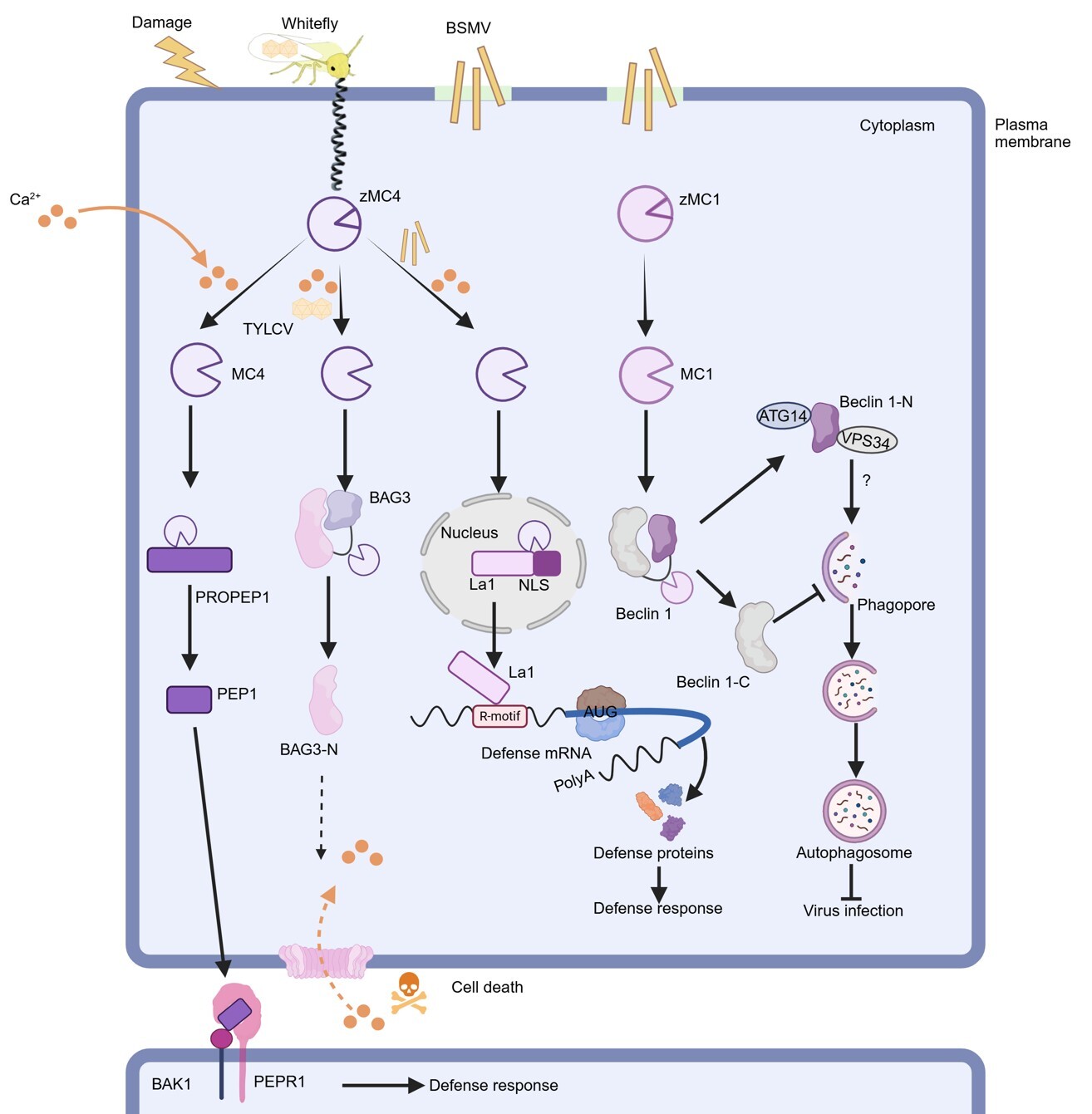
Metacaspase介导的植物抗病毒免疫机制
中国科学院微生物研究所博士研究生梁琳为该文第一作者,叶健研究员为文章通讯作者,博士研究生蒋宇航和王萌蓉参与该综述撰写。该研究获得国家杰出青年科学基金项目及国家重点研发计划的资助。
原文链接:https://doi.org/10.1111/jipb.70259
附件下载: