
- 高级人才招聘
- 中、初级专业技术人才招聘
- 管理、支撑岗位招聘
- 博士后招聘
近日,中国科学院微生物研究所科研团队揭示了B型流感病毒非结构蛋白实现天然免疫逃逸与宿主适应的全新分子机制,这一发现为理解病毒的毒力演化提供了关键的分子基础。
流感病毒长期在人类与多种动物宿主间传播,其持续的适应性进化是导致季节性流感每年反复流行,并在特定条件下引发全球大流行的关键因素。在宿主适应性免疫(如抗体)选择压力下,病毒表面抗原蛋白(以HA和NA为主)常在关键抗原表位附近累积点突变,从而削弱抗体对病毒的识别能力,实现免疫逃逸。然而,病毒如何响应天然免疫压力、实现适应性进化的具体分子机制仍缺乏系统而清晰的阐释。
该研究发现,在B型流感病毒中,NS1蛋白第247位氨基酸发生了由苯丙氨酸(F)向亮氨酸(L)的渐进式替代。近二十多年来,携带L247的病毒占据了绝对的优势地位(图1)。功能研究表明,近期毒株中携带L247的NS1蛋白能够与TUFM及LC3B结合,诱导线粒体自噬,进而通过降解宿主抗病毒“警报器”MAVS抑制I型干扰素的产生。相比之下,早期毒株中F247形式的NS1蛋白几乎无法触发这一自噬依赖的MAVS降解通路(图2)。该突变很可能是B型流感病毒为适应宿主免疫环境、维持其在人群中长期传播所采取的关键进化策略之一。上述结果揭示了天然免疫压力驱动病毒适应性进化与免疫逃逸的新路径,为理解病毒持续传播的进化策略,以及开发靶向免疫逃逸的新型防控手段提供了重要理论支撑。
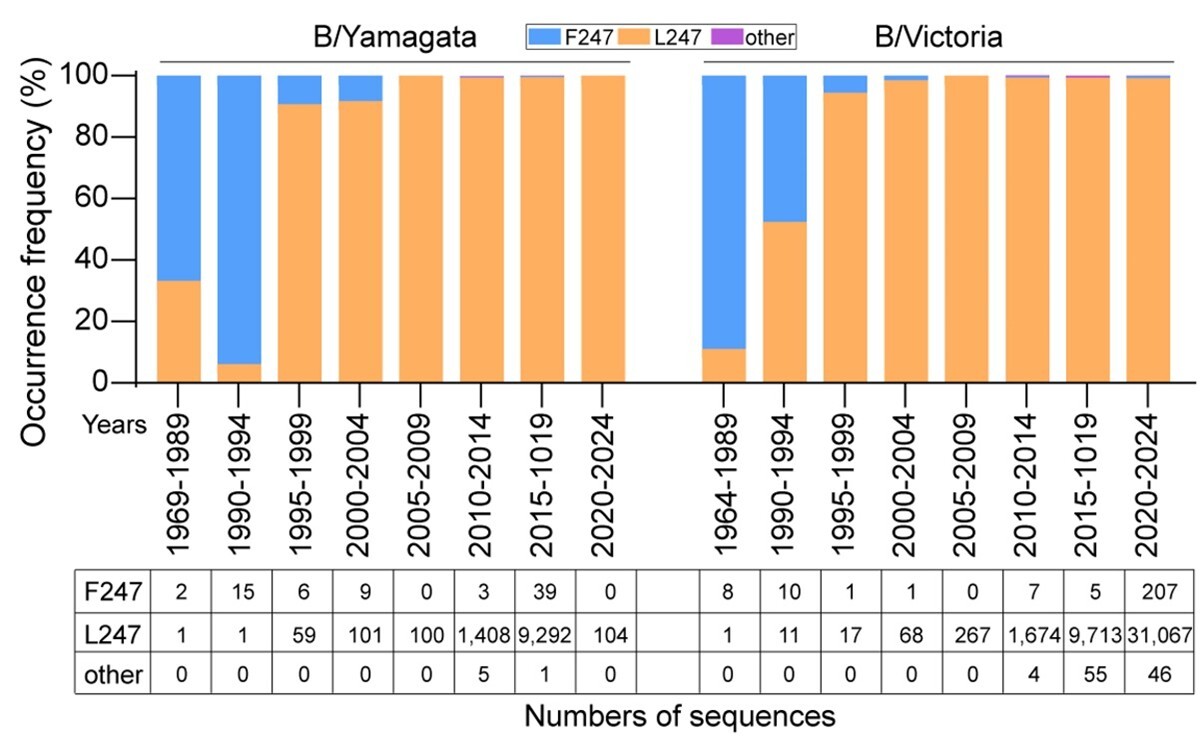
图1. B型流感病毒NS1蛋白247位点的适应性进化分析
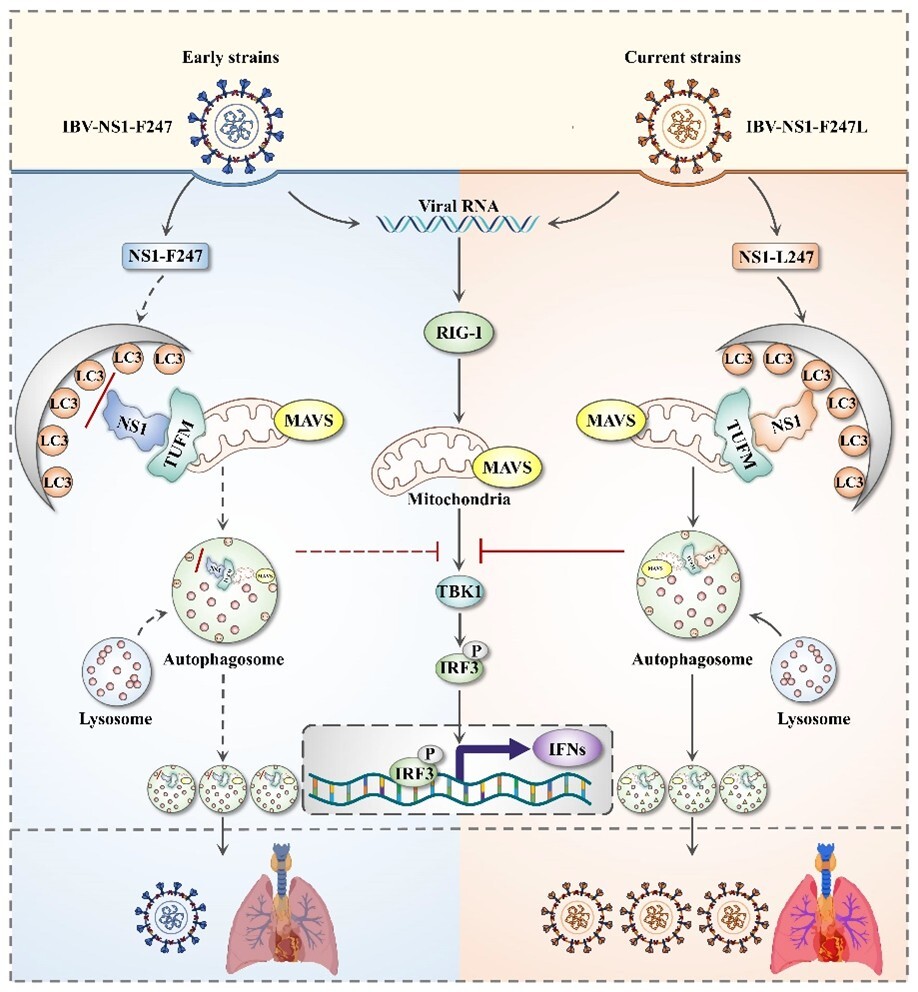
图2. B型流感病毒NS1蛋白的单点突变通过诱导线粒体自噬逃逸宿主天然免疫
微生物所原特别研究助理焦鹏涛、贾潇潇、白晓园及微生物所研究助理赵雨娜博士为论文共同第一作者,微生物所孙蕾项目研究员为论文通讯作者,微生物所刘文军研究员、毕玉海研究员和中国疾病预防控制中心王大燕研究员对本研究提供了重要帮助。该研究得到国家自然科学基金和国家重点研发计划等项目资助。
论文链接:https://www.nature.com/articles/s41467-026-70211-x
附件下载: