结核分枝杆菌(M. tuberculosis, Mtb)感染引起的结核病(Tuberculosis, TB)是重要的致死性慢性传染病,严重威胁全球人类健康。据世界卫生组织(WHO)报道,2019年全球约有1000万新发TB患者,约有141万人死于TB。Mtb是一种兼性胞内寄生菌,其能够运用多种策略干预宿主细胞的正常功能从而逃逸宿主免疫反应,进而实现其在宿主细胞的长期存活。中国科学院微生物研究所刘翠华研究组长期致力于研究Mtb等重要病原菌感染与宿主免疫调控新机制,尤其聚焦Mtb通过劫持宿主泛素系统实现免疫逃逸的新机制以及宿主泛素系统促进抗感染固有免疫功能的分子机制,近年来先后在Nature Immunology、Nature Communication、Proc Natl Acad Sci、Cellular & Molecular Immunology等杂志发表系列研究工作,揭示了病原菌与宿主间相互博弈的动态过程及分子机理,为抗结核治疗及药物研发提供了新思路和特异靶点。
Mtb编码一系列真核样磷酸酶/激酶家族蛋白,其中真核样酪氨酸磷酸酶PtpA和真核样丝氨酸/苏氨酸蛋白激酶PknG均为分泌性效应蛋白,且与Mtb的胞内存活过程密切相关,因此Mtb PtpA和Mtb PknG一直是研发抗结核新药的潜在重要靶点,但目前关于其调控宿主免疫功能的具体机制,包括相关的细胞生物学过程、关键信号通路和靶点,以及所涉及的蛋白间互作和生化调控机制尚未完全明确。因此,深入研究Mtb PtpA和Mtb PknG干扰宿主免疫反应的分子机理,将有利于提供基于Mtb-宿主细胞互作界面的抗结核新靶点,为新型结核病预防及治疗药物和疫苗的开发提供新策略。刘翠华研究组以往研究发现Mtb PtpA与宿主泛素(Ub)相互作用,并先后揭示了Mtb PtpA通过在细胞质俘获Ub激活自身磷酸酶活性以抑制宿主固有免疫反应的分子机制(Nature Immunology, 2015),以及Mtb PtpA在细胞核以泛素非依赖的形式促进肿瘤细胞增殖的分子机制(Nature Communications, 2017)。
近期,刘翠华研究组与北京师范大学邱小波教授团队以及微生物研究所高福院士团队的最新合作研究揭示了Mtb PknG可与宿主泛素系统的另一种关键蛋白—泛素耦合酶(E2)UbcH7发生特异性结合,并催化一种非经典的两步泛素化级联反应来靶向调控宿主泛素系统,进而抑制宿主的固有免疫应答。具体来说,Mtb PknG同时具有非经典的泛素激活酶(E1)和泛素连接酶(E3)活性,并可利用其双功能酶活性促进宿主细胞中的肿瘤坏死因子受体相关因子2(TRAF2)和TGF-β激活激酶1(TAK1)的泛素化及降解,最终抑制NF-κB固有免疫信号通路的活化。
本研究的关键创新点和科学意义为:
1)首次发现了Mtb 中同时具有E1和E3活性的效应蛋白PknG及其靶向的宿主蛋白底物(TRAF2和TAK1)。
2)揭示了Mtb调控的泛素化过程可以由两步级联反应催化实现。经典的泛素化修饰是一个由E1、E2和E3依次催化的三步酶促级联反应,而PknG则可通过两步介导底物的泛素化修饰。在一步反应中,PknG通过其新型的Ubl结构域与UbcH7互作,并作为E1促进Ub与 UbcH7的共价结合,同时可进一步利用其异肽酶活性催化Ub自UbcH7-Ub复合物上解离以获得活化的Ub。有趣的是,PknG直接催化Ub以异肽键的形式结合至UbcH7的Lys82位点,其间无需形成硫酯键连接的PknG-Ub中间体,而经典的E1通常催化Ub以硫酯键的形式结合至UbcH7的Cys86位点,且其间需要形成硫酯键连接的E1-Ub中间体。在第二步反应中,PknG可作为E3将活化的Ub转移至底物蛋白上,并促进它们的泛素化降解。
3)阐明了原核生物调控宿主泛素化过程的特殊能量来源。经典E1活化Ub的过程经常利用ATP水解为AMP来提供能量,而PknG促进Ub活化的能量来源于ATP水解为ADP所释放的能量。综上,本研究的创新性成果刷新了对已有泛素化催化机制的认识,揭示了一种病原菌靶向宿主泛素系统的新策略,提供了基于病原-宿主界面的抗结核治疗新靶点(即Mtb PknG的非经典E1和E3酶活相关的Ubl结构域,该结构域与非致病性分枝杆菌及宿主细胞间几乎无同源性)(图1)。
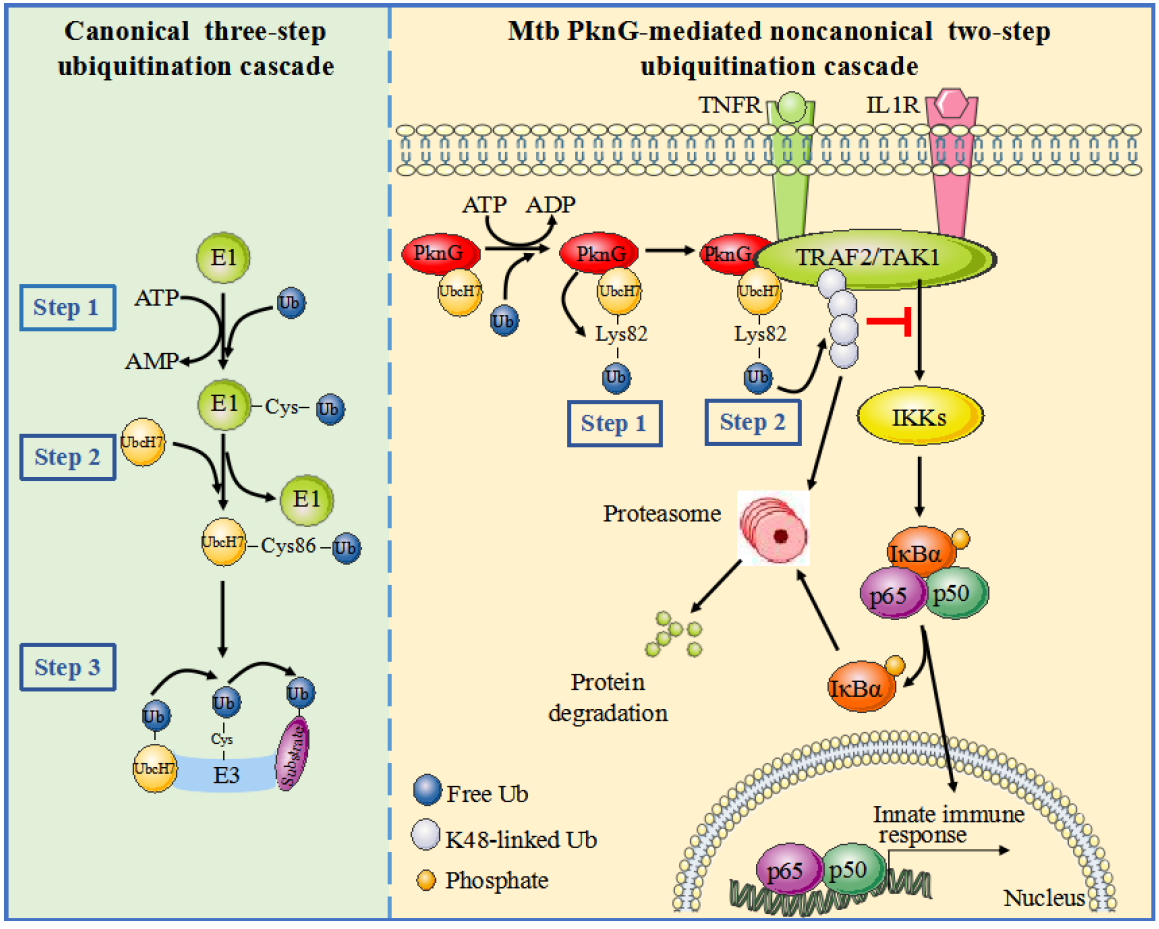
图1. Mtb PknG通过催化非经典的两步泛素化级联反应抑制宿主固有免疫的模式图
相关研究结果已在线发表于国际权威期刊EMBO reports上,题为“M. tuberculosis protein kinase G impairs host immunity by acting as an unusual ubiquitinating enzyme”。刘翠华研究组的项目研究员汪静、博士研究生葛浦浦和硕士研究生雷泽慧为该论文的共同第一作者,中国科学院微生物研究所刘翠华研究员、北京师范大学邱小波教授以及中国科学院微生物所高福院士为本文的共同通讯作者。该研究得到国家自然科学基金委、中国科学院战略性先导科技专项(B类)、国家重点研发计划项目、国家科技重大专项以及中国科学院青年创新促进会人才项目的资助。
文章链接:http://doi.org/10.15252/embr.202052175




