高致病性禽流感H5N1病毒严重威胁公共卫生安全。H5N1病毒在跨宿主传播过程中,其聚合酶蛋白的适应性突变是影响病毒复制的关键因素,但牛源H5N1病毒聚合酶发生哪些宿主适应性突变及其生物学功能尚未完全阐明。
2025年12月20日,中国科学院微生物研究所邓涛团队与高福院士团队合作在Nature Communications在线发表了题为Emergence of mammalian-adaptive PB2 mutations enhances polymerase activity and pathogenicity of cattle-derived H5N1 influenza A virus 的研究论文。该研究系统鉴定了H5N1病毒从禽向牛跨种传播过程中,其聚合酶PB2蛋白发生的哺乳动物适应性关键突变,揭示了突变通过增强病毒聚合酶对哺乳动物宿主因子ANP32A的利用效率,从而提升病毒在哺乳动物中的复制水平与致病力。
研究发现,PB2蛋白是决定牛源病毒在哺乳细胞高效复制的关键因素,其中PB2 M631L突变能显著增强聚合酶活性。回溯分析显示,PB2 M631L并非首次出现,早在2013-2014年柬埔寨和越南的H5N1人类感染病例中已经出现,提示其在H5N1病毒跨种感染中发挥重要作用但相关风险长期被低估。小鼠感染实验证实,携带PB2 M631L的病毒可引起严重肺部感染并导致高死亡率,其致病力与经典哺乳动物适应性突变PB2 E627K相当;当两者共存时,病毒致病力呈现协同增强效应。
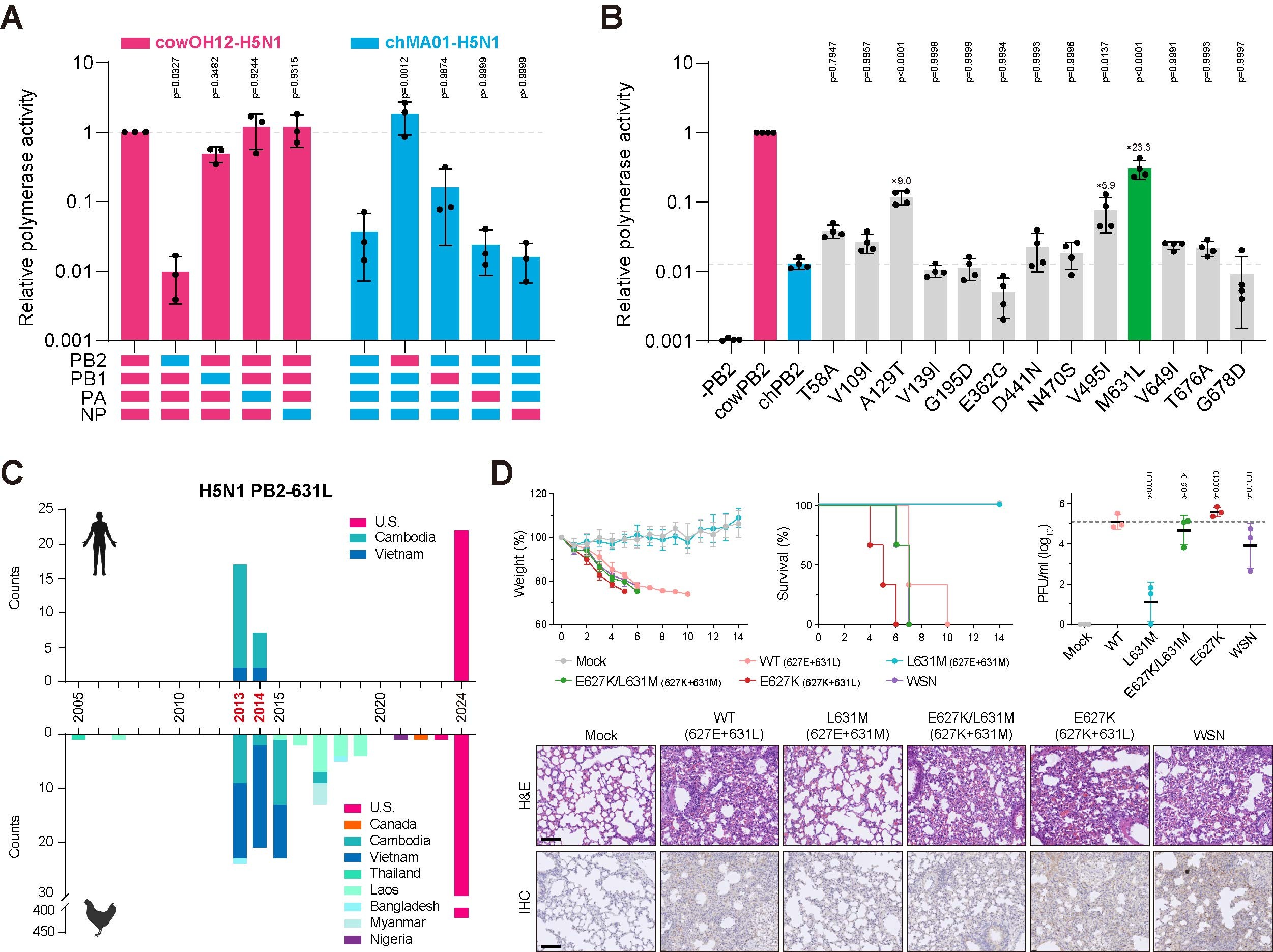
图1 H5N1关键氨基酸突变PB2 M631L增强病毒复制能力和致病性
研究进一步发现,H5N1病毒在持续传播过程中,除出现E627K、Q591R、D701N等已知突变外,还出现了I647V、G685R、K736R等多个新型适应性突变,这些突变均能增强病毒聚合酶在哺乳细胞中的活性。结构分析表明,这些突变通过增强对牛和人源ANP32A/B的利用效率,从而提高病毒在哺乳动物体内的复制能力与致病性。
该研究不仅为理解H5N1病毒在哺乳动物中的快速适应与进化提供了关键分子证据,也揭示了PB2 M631L这一历史上曾被低估的适应性突变位点的重要性。上述发现突显了持续监测H5N1病毒在禽类和哺乳动物宿主中遗传变异的紧迫性,对科学评估其大流行风险及制定预警与防控策略具有重要参考价值。
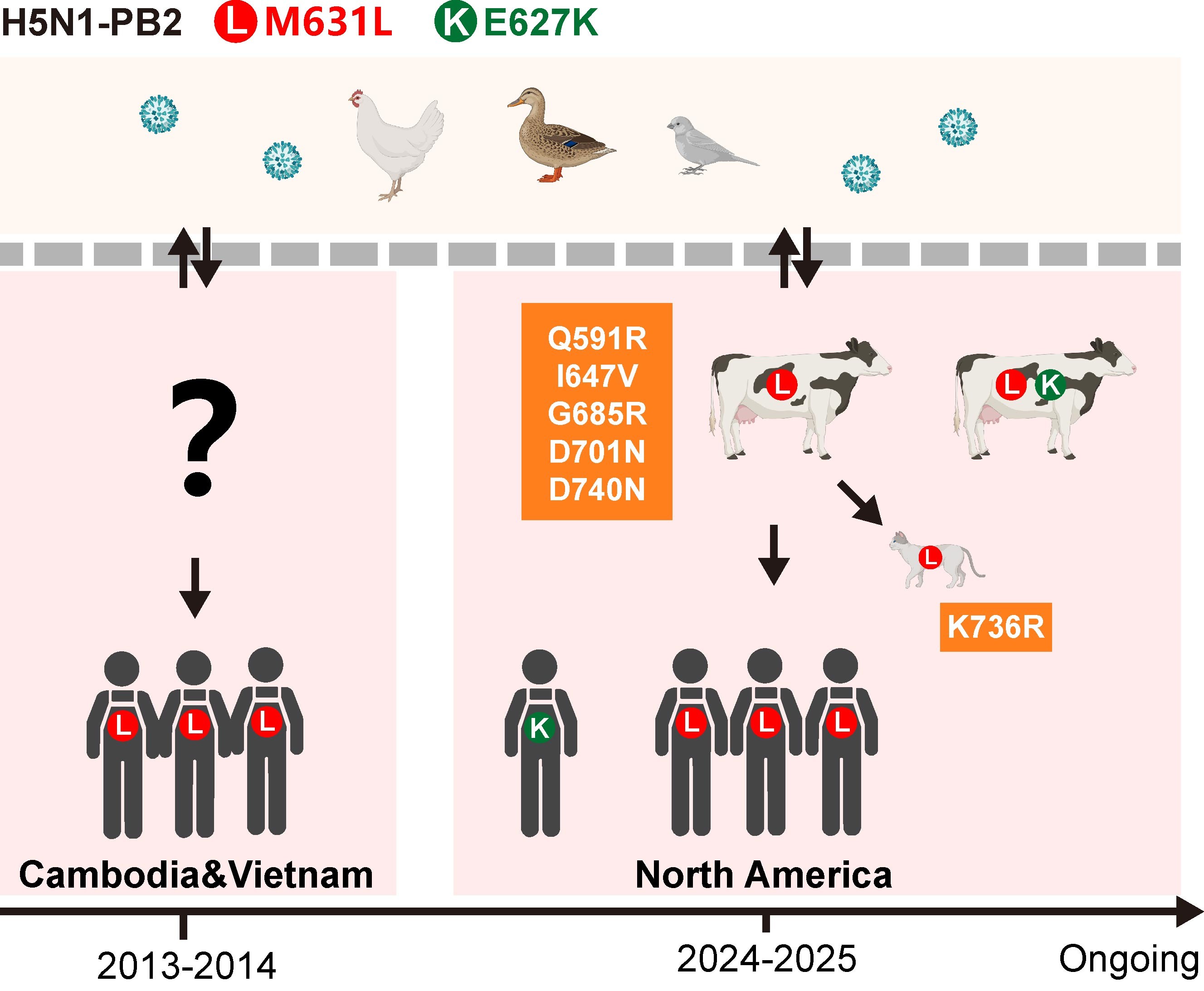
图2 H5N1病毒聚合酶PB2蛋白关键突变参与病毒跨种传播
原文链接:https://www.nature.com/articles/s41467-025-67753-x




