在自然界中,具有混杂催化功能的蛋白质在自然选择的压力下能够趋异进化为活性更高或功能更专一的不同蛋白质。将趋异进化概念应用到蛋白质的定向进化工程改造中,能够将天然蛋白改造成为底物专一性各不相同的多种蛋白。定向趋异进化即是在定向进化和趋异进化理论上建立的一种重新设计酶的催化功能的蛋白质工程学方法。
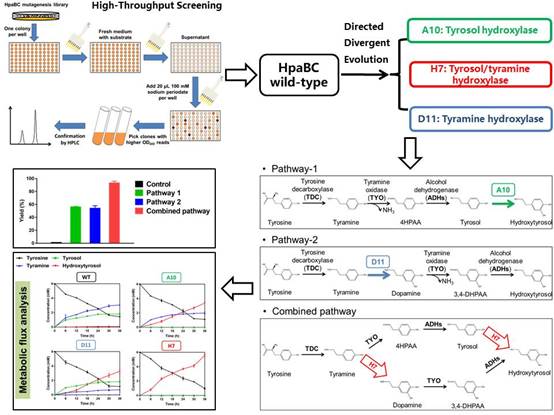
羟基酪醇(Hydroxytyrosol),主要存在于橄榄属植物的果实和枝叶中,是一种天然的强抗氧化剂,具有很强的清除自由基能力,可预防自由基引起的直接损伤以及紫外线诱导的氧化应激等。此外研究报道羟基酪醇还具有很好的抗肿瘤活性及降血脂、抗动脉硬化、治疗糖尿病和肥胖症、抗菌消炎等功效。已报道的以酪氨酸为底物生产羟基酪醇的生物合成途径由于需要酪氨酸羟化酶及四氢生物蝶呤循环系统,造成羟基酪醇的生物合成效率低下,羟基酪醇产量很低(29 mg/L),而底物转化率不足20%。唐双焱课题组在文献调研的基础上,用同一套途径酶设计了两条不同的以酪氨酸为底物生产羟基酪醇的生物合成途径。研究发现当两条途径同时工作时,羟基酪醇的生物合成效率大大提高。因此在前期工作基础上,唐双焱团队利用蛋白质定向趋异进化策略对大肠杆菌单加氧酶HpaBC进行了改造,获得了分别具有酪醇羟化酶,酪胺羟化酶及酪醇/酪胺羟化酶混杂催化活性的三个优良突变体A10,D11和H7,这些突变体能够有效催化羟基酪醇新生物合成途径中天然缺失的步骤。研究表明具有酪醇/酪胺羟化酶混杂催化活性的HpaBC突变体H7能够有效减少蛋白质过表达造成的细胞代谢负担,并能实现生物合成碳流在两条途径之间的高效分配,从而通过对多条合成途径间代谢流的重排显著提高羟基酪醇生物合成效率。在没有进行发酵条件优化的情况下,羟基酪醇产量达到1890 mg/L,转化率可达到82%。代谢工程通常聚焦于单条合成途径中酶的调控,唐双焱团队的该项工作展示了基于酶的混杂催化活性设计多条合成途径,通过减少细胞代谢负担并实现碳流的重排,实现羟基酪醇的高效生物合成,进一步拓展了蛋白质定向进化手段在代谢工程研究中的应用,为天然产物生物合成途径的设计构建提供了新的思路和技术依据。
该研究以“Promiscuous enzymatic activity-aided multiple-pathway network design for metabolic flux rearrangement in hydroxytyrosol biosynthesis”为题,2019年2月27日在线发表于Nature Communications。中国科学院微生物研究所唐双焱组助理研究员陈伟博士、博士研究生姚骏为论文并列第一作者,唐双焱研究员,金建明教授(北京工商大学)和何洋博士(浙江大学)为论文共同通讯作者。研究工作得到了国家自然科学基金青年项目(31501037)及面上项目(31870072,21472234)的资助。
论文链接:https://www.nature.com/articles/s41467-019-08781-2