肠道菌群的结构、功能变化与宿主的生理和病理过程密切相关。肠道菌群被称为人体新的“器官”,被作为药物研发的新“靶标”。大量研究表明肠道菌群紊乱与肥胖、糖尿病和高血脂症的发生、发展密切相关。“哪些共生菌株参与了宿主糖脂代谢的调节,它们的互作机制如何”是微生物组研究的重要科学问题之一。
狄氏副拟杆菌(Parabacteroides distasonis)是人体核心菌群之一,相关性分析表明其含量与肥胖、非酒精性脂肪肝、糖尿病等疾病状态呈显著负相关,提示其可能在糖脂代谢方面发挥正向调节作用。微生物所刘宏伟与刘双江、王军研究团队紧密合作、协同攻关,发现狄氏副拟杆菌可以显著改善高脂饮食诱导肥胖(DIO)小鼠及ob/ob肥胖模型小鼠的肥胖、胰岛素抵抗、脂代谢紊乱及非酒精性脂肪肝症状。通过体内外实验首次发现狄氏副拟杆菌具有广泛的胆酸转化功能,能够水解多种结合型胆酸,同时转化为多种次级胆酸(石胆酸,熊去氧胆酸等);还可以产生大量琥珀酸。石胆酸等次级胆酸通过激活肠道FXR信号通路,改善脂代谢紊乱;熊去氧胆酸可以修复肠壁完整性;琥珀酸通过作用于肠道糖异生(IGN)途径关键酶果糖-1,6-二磷酸酶(FBPase),激活肠道糖异生,从而调节食欲,促进肝脏糖原合成,改善宿主糖代谢紊乱。狄氏副拟杆菌通过产生琥珀酸、次级胆酸通过激活不同的信号通路,发挥多靶点整体调节作用,是一种潜在、新型抗代谢综合症益生菌。
本研究从肠道共生菌代谢产物角度系统揭示了肠道核心菌群狄氏副拟杆菌与宿主互作-调节糖脂代谢的复杂机制,加深了我们对肠道共生菌生理作用及作用机制的理解,首次证明了琥珀酸是果糖-1,6-二磷酸酶的天然配体。靶向肠道糖异生关键酶-果糖-1,6-二磷酸酶的激动剂可以作为新型降糖药物研发。
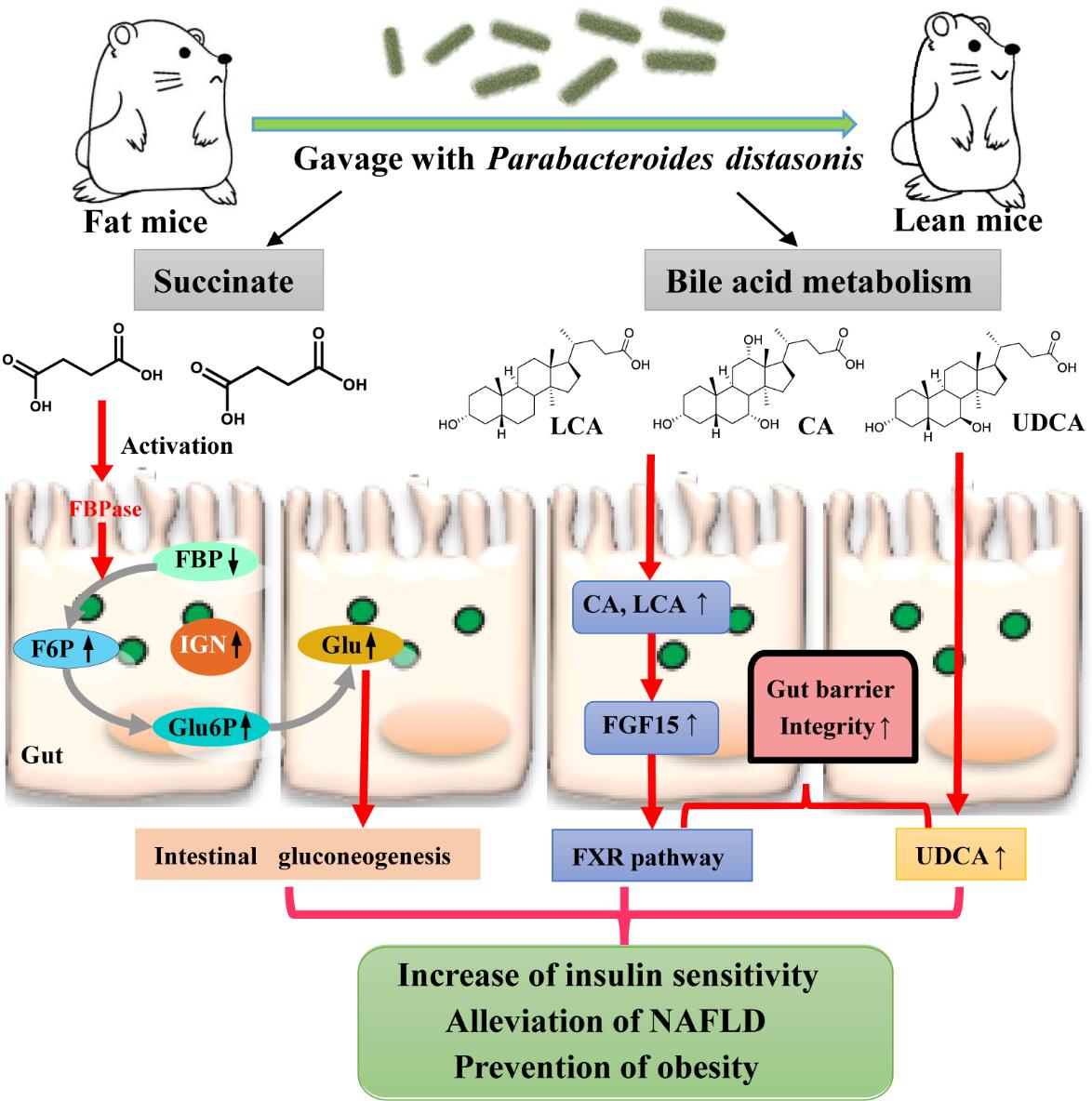
图:肠道共生菌狄氏副拟杆菌(Parabacteroides distasonis)改善代谢综合症的作用机制
以上研究成果以“Parabacteroides distasonis modulates host metabolism and alleviates obesity and metabolic dysfunctions via production of succinate and secondary bile acids”为题在线发表在国际著名学术刊物Cell Reports (2019, 26, 222-235)上。刘宏伟课题组博士研究生汪锴、硕士研究生廖明芳、刘双江课题组周楠助理研究员为该论文的共同第一作者。该研究工作得到了中国科学院重点部署项目 (KFZD-SW-219)、国家自然科学基金 (81773614)和中国科学院青年创新促进会项目 (2014074)的资助。




