作者: 朱宝利 李晶(中国科学院微生物研究所)
来源:《知识就是力量》杂志
在决定吃什么的时候,你选择的理由是什么?是个人喜好,还是实惠的价格,抑或是是否有利于健康?你是否特别喜欢某种食物,或是完全不能接受另外某种食物呢?在选择食物的时候,你是否想过肠道会参与你的决策?带着这些问题,我们来聊聊肠道与食物选择的关系。
我们的祖先在很早以前就已有“食药同源”的说法,通过选择性食用食物而达到强身健体、治疗保健的作用。到了现代,随着物质生活极大丰富,人们更加注重自身的保健,“养生”被经常挂在嘴边。根据食物与健康的关系,很多食物被贴上了“有益”或“有害”的标签。一般来说,食物对自身健康的好坏、对疾病的缓解或治疗,主要是针对食物中的某些特殊成分对人体免疫系统、消化系统及内分泌系统的作用而言的。
近几年,随着人类对肠道微生物的逐渐认识,仿佛打开了“潘多拉魔盒”,原来这群相伴我们一生的微生物群体与我们生老病死、喜怒哀乐、昼夜更替都有紧密的联系。
肠道就像是一个“超级工厂”,微生物细胞就如同流水线上的工人,它们根据自身携带的功能基因,选取所需加工的原料,一刻不停地进行合成和分解代谢,将各种食物大分子降解后分泌代谢产物,最终通过肠道黏膜、血液等途径运送到身体各个部分发挥作用。
可以想象一下,如此庞大而复杂的工厂中,某一个环节一旦出现问题,则一定会对机体产生负面影响,从而患病。早在公元前300多年,现代医学先驱希波克拉底就已预言“所有疾病都源于肠道”,且“死亡开始于肠道”。人类通过2000多年的实践,也验证了希波拉底的预言,发现在健康状态与疾病状态下,肠道微生物结构存在着显著的变化。
吃出来的肠道Bug
随着生活水平的提高,肥胖问题日渐凸显。我们通常认为这是吃出来的一种亚健康的身体状态。经过科学家的研究发现,肥胖人群的肠道微生物菌群结构与健康人群存在显著差异,肠道微生物处于失衡的状态。对比发现,肥胖人群的肠道菌在“门”水平上与健康人就已经存在差异了。注意了,“门”可是细菌分类的最高级别;换句话说,从“根儿”上就有所不同了!就菌群的多样性来说,肥胖人群的菌群多样性显著低于健康人群,这就意味着面对同样的食物,肥胖者的消化代谢功能将会与健康人存在差异,可能某些重要的代谢途径存在缺失或异常。
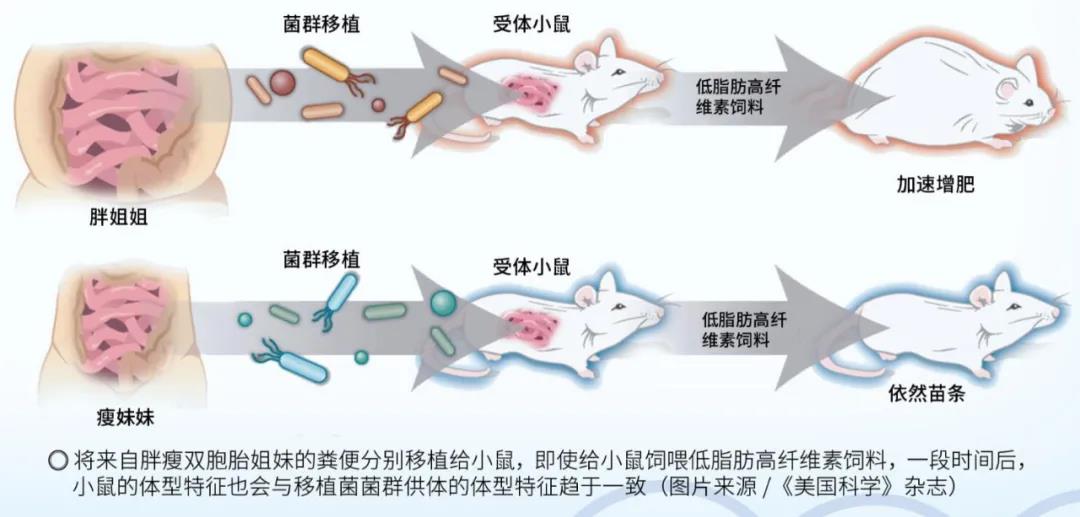
科学家将肥胖病人的粪便移植给无菌小鼠并饲喂高脂肪低纤维素饲料,小鼠出现了肥胖及胰岛素抵抗的症状,说明其代谢功能已发生改变。若将胖瘦不同的双胞胎姐妹的粪便移植给无菌小鼠,即使给予高纤维低脂肪的“健康食品”,移植了胖姐姐粪便的小鼠仍比移植了瘦妹妹粪便的小鼠胖,说明肠道微生物在代谢过程中发挥着重要的作用。如果让胖小鼠和瘦小鼠“同居”一段时间,胖小鼠居然变瘦了!分析其肠道微生物菌群结构发现,其菌群多样性升高了。在对人群的研究中,科学家要求肥胖人群每日定量摄入牛油果,经过为期12周的干预,摄入组菌群多样性增加,可发酵膳食纤维的粪杆菌属、毛螺菌属等细菌得到富集,粪便中脂肪酸浓度升高而胆汁酸浓度降低。这就意味着其肠道Bug得到了修复,改善了身体状况。
肠道细菌也挑食
在以上一系列实验中,肠道微生物菌群发生改变,一定存在着某些菌的丰富度升高而另一些菌的丰富度下降的现象。那么在修复肠道Bug的过程中,这些好的菌是如何胜出的呢?
早在研究“同居”小鼠的实验中,科学家就已经发现只有给小鼠饲喂低脂肪高纤维的饲料时,胖小鼠肠道内的某些拟杆菌(Bacteroides)增殖了,这就意味着这些拟杆菌可能偏爱吃纤维。

为了验证这个想法,科学家再次启用胖瘦双胞胎,将瘦妹妹粪便中分离出的20种细菌移植到无菌小鼠体内,其中包括4种有助于胖小鼠减肥的拟杆菌;然后又配制出含34种高膳食纤维的健康食品。在实验中先给小鼠喂高脂低纤维的不健康食品,让定植的20种细菌的结构发生改变,抑制喜欢膳食纤维的拟杆菌增殖。
然后再给它们喂配制的健康饲料,从肠道菌群的变化了解肠道微生物对食物的偏好。实验结果发现,就像人一样,当自己喜欢的食物较多时,细菌就会猛吃而加速繁殖,其在肠道中的菌群丰富度也会相应增加。
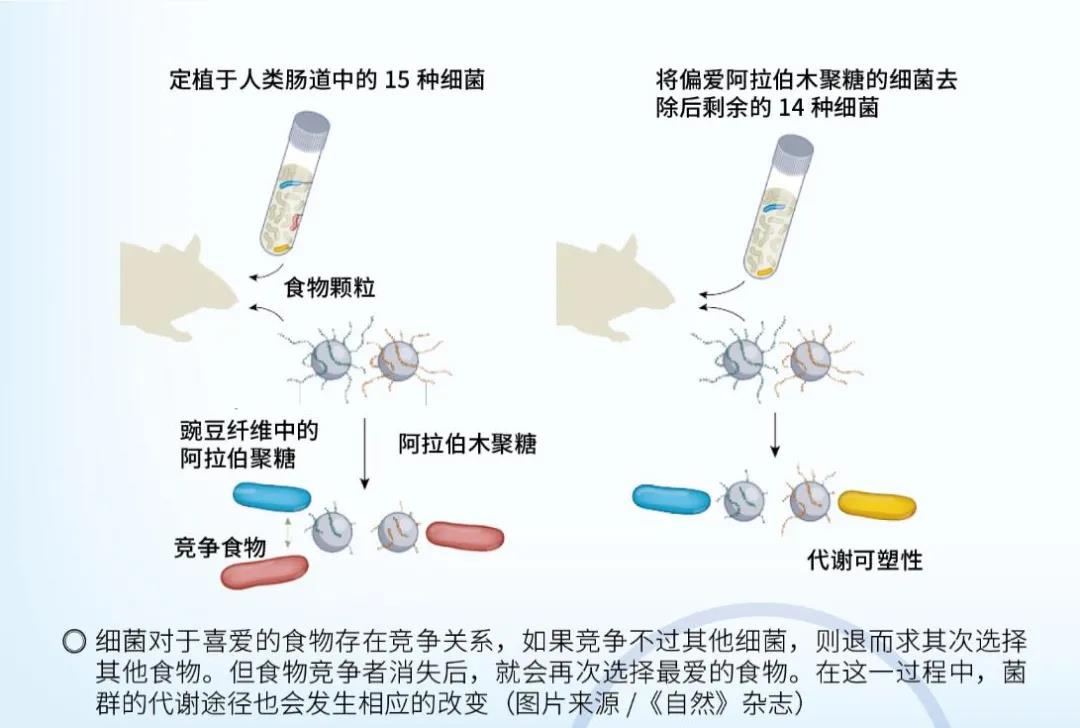
对于研究者特别关注的具有减肥功能的4株细菌,它们根据自身携带的功能基因不同,对不同的食物喜好度也存在差异。但是问题又来了,食物还是那么多,爱吃这种食物的细菌不断增殖时,面临“狼多肉少”的局面,细菌该怎么办?
科学家采用带荧光的人工食物颗粒饲喂小鼠,监测肠道菌的代谢能力时发现,那些“能抢的”细菌还继续吃最爱的食物,而“竞争力稍差的”细菌只能退而求其次吃其他的食物,说明细菌对食物的偏好是可以依据食物的多少而发生改变的。同时也说明了,肠道微生物具有很强的可塑性,可以依据食物的改变而改变。可以说,肠道有Bug不用慌,还能治!
被细菌安排的饮食结构
既然食物可以影响肠道微生物的菌群结构,也通过引发微生物竞争而改变微生物对食物代谢的偏好性,那么反之,肠道微生物是否会影响宿主对食物的偏好性呢?
科学家以秀丽线虫作为研究对象展开研究。首先发现某些细菌可以引发线虫对于某些挥发性化学物质(如异戊醇)表现出强烈喜爱,同样对于某些化学物质(如辛醇)表现出厌恶。当特定菌株JUb39被定植于线虫肠道后,线虫食量不减的同时对于辛醇的厌恶程度大大降低。
通过对JUb39的基因组分析发现,由于其基因组中存在编码酪氨酸脱羧酶基因,可产生酪胺以弥补线虫自身对酪胺合成的需求;细菌产生的酪胺又可被线虫代谢为章鱼胺后结合在特定的神经细胞受体上,从而调节线虫对辛醇的厌恶反应。
在这项研究中,JUb39利用自身产生的酪胺绕过了宿主产生酪胺这一步,巧妙地利用了同源分子的功能,改变了宿主的喜好。并且线虫的肚子里一旦有JUb39定植,线虫就会开始“挑食”优先选择这种细菌为食。

虽然在线虫实验中人们发现了肠道微生物调控宿主对食物的偏好性,但对于人类、小鼠等动物而言,其自身结构复杂,肠道微生物种类多样,特别是人类生活环境纷繁复杂,食物多种多样,解开挑食之谜还需要一个漫长的过程。
但是值得注意的是,已有大量的研究发现,食物的单一化将会改变肠道菌群的结构、降低菌群多样性,造成某些代谢途径的改变。

在儿童营养状态的相关研究中,孟加拉、秘鲁等不发达国家和地区的儿童在幼年罹患营养不良,造成其肠道菌群建立滞后,血项指标、代谢物指标及生理指标均落后于正常儿童。
即使后期进行饮食干预补充膳食纤维,虽然能有效改善其生长、发育及免疫功能等生理指标,但是在幼年时期造成的某些共生肠道菌缺失,在后期是再无法获取的,直至成年后仍与健康人存在差异。
在动物实验中甚至还发现,这种肠道菌缺失的Bug,具有遗传性。不得不说,合理饮食,均衡营养,绝不是你一个人的事!




